Ново изследване насочва вниманието към имунен протеин, който може да играе ключова роля в разпространението на мозъчните увреждания при болестта на Паркинсон. Протеинът, известен като GPNMB или glycoprotein nonmetastatic melanoma B, се свързва с процеса, при който патологични натрупвания на алфа-синуклеин преминават от една нервна клетка към друга и постепенно засягат различни области на мозъка.
Това откритие е важно, защото днешното лечение на болестта на Паркинсон основно облекчава симптомите, но не спира самото развитие на заболяването. Медикаменти като леводопа могат значително да подобрят двигателните прояви, а при определени пациенти дълбоката мозъчна стимулация може да намали част от тежките симптоми. Въпреки това медицината все още не разполага с доказано лечение, което надеждно да забавя или спира невродегенеративния процес.
Именно затова всяка потенциална мишена, свързана с ранното разпространение на патологичния процес, представлява сериозен интерес. Новите данни предполагат, че блокирането на GPNMB чрез моноклонални антитела може да прекъсне един самоподдържащ се механизъм на увреждане в мозъка.
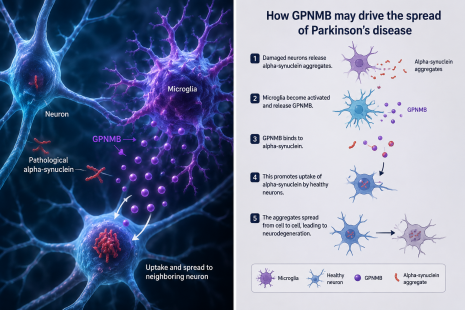
Какво се случва в мозъка при болестта на Паркинсон
Болестта на Паркинсон е хронично прогресиращо невродегенеративно заболяване, при което постепенно се увреждат нервни клетки, участващи в контрола на движенията. Най-известният процес е загубата на допамин-продуциращи неврони в областта substantia nigra, но заболяването не се ограничава само до тази зона.
С напредването си Паркинсон засяга различни мозъчни мрежи и може да доведе не само до тремор, скованост и забавени движения, но и до нарушения на съня, промени в настроението, когнитивни проблеми, затруднено преглъщане, автономни симптоми и повишен риск от деменция.
Един от централните биологични белези на заболяването е натрупването на неправилно нагънат алфа-синуклеин. Това е белтък, който нормално участва в работата на нервните окончания, но при Паркинсон може да образува патологични агрегати. Тези агрегати се натрупват в невроните и се свързват с тяхната дисфункция и загиване.
Смята се, че част от патологичния алфа-синуклеин може да се освобождава от увредени клетки и да бъде поеман от съседни неврони. Така процесът постепенно се разпространява в мозъка, подобно на верижна реакция.
Каква е ролята на GPNMB
Новото изследване поставя GPNMB в центъра на този процес. Според учените протеинът се произвежда в значителна степен от микроглията – имунните клетки на мозъка. Микроглията обикновено има защитна функция: тя разпознава увреждания, премахва клетъчни отпадъци и участва в поддържането на мозъчната среда.
Когато обаче микроглията се намира в близост до увредени или загиващи неврони, тя може да започне да произвежда по-големи количества GPNMB. Част от този протеин се отделя от повърхността на клетките и започва да циркулира в междуклетъчното пространство.
Според изследователите именно секретираната форма на GPNMB може да улесни поемането на фибриларен алфа-синуклеин от други нервни клетки. Това означава, че имунната реакция, която първоначално би трябвало да бъде защитна, може неволно да ускори разпространението на патологичния процес.
Така се оформя опасен цикъл: алфа-синуклеинът уврежда невроните, увредените неврони активират микроглията, микроглията освобождава GPNMB, а GPNMB подпомага по-нататъшното разпространение на алфа-синуклеиновата патология.
Моноклонални антитела като възможен подход
Една от най-важните части на изследването е, че учените са разработили антитела, които блокират GPNMB в предклинични модели. В експерименти с култивирани неврони тези антитела са успели да предотвратят разпространението на алфа-синуклеиновата патология от клетка към клетка.
Това не означава, че вече има готово лечение за пациенти, но е силен сигнал, че GPNMB може да бъде реалистична терапевтична мишена. Моноклоналните антитела вече са утвърден клас медикаменти в онкологията, ревматологията, гастроентерологията, неврологията и други области. Те могат да бъдат разработени така, че да разпознават много специфични молекули и да блокират тяхната функция.
При Паркинсон подобен подход би имал различна цел от стандартното симптоматично лечение. Вместо да се компенсира недостигът на допамин, терапията би се опитала да прекъсне самия механизъм на разпространение на мозъчното увреждане.
Защо това може да е важно в ранните стадии
Най-големият потенциал на подобна стратегия вероятно е в ранните стадии на заболяването. При много пациенти диагнозата се поставя, когато двигателните симптоми вече са видими, но мозъчният процес е започнал години по-рано.
Ако бъде разработена терапия, която забавя разпространението на алфа-синуклеиновата патология, тя би могла да има най-голям ефект преди да са настъпили тежки и необратими увреждания. Това е една от причините в съвременната неврология да се търсят не само нови лекарства, но и ранни биомаркери за диагностика и проследяване.
За пациентите подобна терапия би означавала не просто по-добър контрол на тремора или сковаността, а потенциално по-бавно влошаване на заболяването, по-дълго запазване на функционалността и по-късно развитие на тежки усложнения.
Доказателства от човешка мозъчна тъкан
За да проверят дали лабораторните резултати имат значение при хора, изследователите са анализирали тъкан от голяма мозъчна банка. Данните показват, че хора с генетични варианти, свързани с по-висока продукция на GPNMB, имат по-изразена алфа-синуклеинова патология.
Това е важна стъпка, защото много потенциални терапии изглеждат обещаващи в клетъчни модели, но не се потвърждават при човешко заболяване. В случая връзката между GPNMB и патологичните промени в човешки мозък подсилва аргумента, че протеинът не е страничен наблюдател, а може да участва активно в прогресията.
Допълнително значение има и фактът, че повишените нива на GPNMB не са били свързани по същия начин с маркери на други невродегенеративни заболявания като Алцхаймер. Това подсказва, че механизмът може да има по-специфична връзка с Паркинсон и алфа-синуклеиновата патология.
Какво означава това за съществуващото лечение
Днешните терапии при Паркинсон остават изключително важни. Леводопа продължава да бъде златен стандарт за контрол на моторните симптоми, а допаминовите агонисти, MAO-B инхибиторите, COMT инхибиторите и други лекарства имат място според стадия и конкретния пациент.
При част от болните дълбоката мозъчна стимулация може значително да намали моторните флуктуации и дискинезиите. Физиотерапията, двигателната активност, логопедичната рехабилитация, контролът на съня и храненето също са важни елементи от дългосрочната грижа.
Ограничението е, че тези подходи основно управляват проявите на заболяването. Те не са насочени към спиране на разпространението на алфа-синуклеиновата патология в мозъка.
Затова GPNMB представлява интерес именно като възможна disease-modifying мишена – тоест мишена за терапия, която би могла да промени хода на заболяването, а не само да облекчи симптомите.
Имунната система като нов фронт в лечението на Паркинсон
Дълго време Паркинсон се разглеждаше предимно като заболяване на допаминовите неврони. Днес картината е много по-сложна. Все повече данни показват, че имунната система на мозъка, възпалението, митохондриалната дисфункция, чревно-мозъчната ос и генетичните фактори участват в развитието и прогресията на заболяването.
Микроглията вече не се възприема просто като пасивен участник, който реагира на увреждането. Тя може активно да оформя хода на невродегенеративния процес. В някои ситуации микроглиалната реакция е защитна, но при хронична активация може да поддържа възпаление и да засилва увреждането.
Откритието за GPNMB се вписва именно в тази по-нова концепция. То показва, че една имунна молекула може да се окаже мост между клетъчното увреждане, микроглиалната реакция и разпространението на патологични белтъчни агрегати.
Какви са ограниченията на откритието
Въпреки обещаващите резултати, изследването все още не означава, че пациентите скоро ще получат ново одобрено лечение. Данните са предклинични и трябва да бъдат потвърдени в следващи етапи.
Предстоят няколко ключови въпроса:
- дали блокирането на GPNMB е безопасно при хора;
- дали антителата могат да достигат ефективно до нужните зони в мозъка;
- дали терапията ще има ефект при вече диагностицирани пациенти;
- дали ще е най-полезна в ранни, продромални или по-късни стадии;
- дали GPNMB може да се използва и като биомаркер за прогресия;
- какви странични ефекти могат да възникнат при дългосрочно блокиране на протеина.
Историята на невродегенеративните заболявания показва, че преходът от лабораторна идея до ефективна терапия е труден. Много обещаващи молекули са се проваляли в клинични изпитвания, особено когато заболяването вече е напреднало.
Именно затова откритието трябва да се разглежда като важна научна стъпка, но не и като готово лечение.
Глобалното значение на проблема
Болестта на Паркинсон е едно от най-бързо нарастващите неврологични заболявания в света. Застаряването на населението, по-дългата преживяемост и по-доброто разпознаване на симптомите водят до увеличаване на броя диагностицирани пациенти.
Заболяването носи сериозна тежест не само за пациентите, но и за семействата, здравните системи и социалните услуги. С напредването му нуждата от грижи нараства, а качеството на живот може значително да се влоши.
В този контекст разработването на терапии, които забавят прогресията, е един от най-важните приоритети в неврологията. Дори умерено забавяне на заболяването би могло да има голям ефект върху независимостта на пациентите и разходите за дългосрочна грижа.
Какво означава това за България
За България подобни научни разработки са важни по няколко причини. Населението застарява, а невродегенеративните заболявания постепенно ще заемат все по-голям дял от здравните и социалните предизвикателства.
Пациентите с Паркинсон у нас, както и в останалата част на Европа, се нуждаят от по-ранна диагностика, по-добър достъп до специализирана неврологична грижа, рехабилитация и дългосрочно проследяване. Новите disease-modifying подходи, ако бъдат доказани, вероятно ще изискват и по-прецизни диагностични тестове, за да се определя кои пациенти са подходящи за лечение.
Това означава, че бъдещето на терапията при Паркинсон вероятно няма да бъде само в ново лекарство, а в цялостна промяна на модела: ранно откриване, биомаркери, персонализирана оценка на риска и комбинирано лечение.
Перспектива за бъдещето
Откритието за GPNMB добавя нова посока в усилията за разработване на терапия, която променя хода на болестта на Паркинсон. То обединява няколко ключови направления в съвременната медицина: невроимунология, протеинова патология, генетика, моноклонални антитела и персонализирана терапия.
Ако бъдещите изследвания потвърдят, че блокирането на GPNMB може безопасно да забавя разпространението на алфа-синуклеиновата патология, това би било значителна крачка напред. Особено ценно би било подобно лечение да се прилага в ранен стадий, когато невроналната загуба все още не е толкова напреднала.
Засега обаче най-точната оценка е внимателен оптимизъм. Научната основа е силна, но клиничното доказване предстои.
Заключение
Новото изследване поставя GPNMB сред най-интересните нови молекулярни мишени при болестта на Паркинсон. Данните показват, че този имунен протеин може да подпомага разпространението на алфа-синуклеиновата патология в мозъка, а блокирането му с антитела в предклинични модели може да прекъсне процеса.
Това не е незабавно лечение за пациентите, но е важна стъпка към терапия, която би могла да се насочи към причинните механизми на прогресията, а не само към симптомите.
В свят, в който броят на хората с Паркинсон продължава да расте, подобни открития са особено важни. Те показват, че бъдещето на лечението вероятно ще бъде в ранното откриване, прецизните биомаркери и терапии, насочени към конкретните механизми на невродегенерацията.
Източници
Perelman School of Medicine at the University of Pennsylvania
National Institute of Neurological Disorders and Stroke – Parkinson's Disease







Добави коментар
Внимание: Задължително е писането на кирилица.